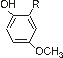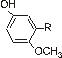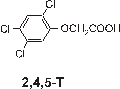Zadanie 6.1
Rozdzielanie izomerów
t-butylohydroksyanizolu
t-butylohydroksyanizol (BHA) jest używany w produkcji żywności jako
antyoksydant. Ma on także właściwości przeciwrakowe. Produkt handlowy jest
mieszaniną dwóch izomerów o wzorach:
|
|
|
|
|
|
|
3-HBA |
2-HBA |
Związek 3-BHA jest ok. 2,4 razy bardziej aktywny jako antyoksydant niż
2-BHA, podczas gdy związek 2-BHA wykazuje silniejsze niż 3-BHA działanie
przeciwrakowe. Potrzebna jest zatem metoda określenia składu BHA. W tablicy podano
czasy retencji 2-BHA i 3-BHA przy różnych składach fazy ruchomej
|
Zawartość
propanolu w wodzie, (% V/V) |
Czas retencji,
min |
|
|
2-BHA |
3-BHA |
|
|
1 |
96 |
47,8 |
|
2 |
30,4 |
21,6 |
|
3 |
17,2 |
13,3 |
|
5 |
10,7 |
9,0 |
|
7 |
8,2 |
7,0 |
|
10 |
6,8 |
6,0 |
Warunki:
kolumna 250x4,6mm
przepływ 1ml/min
porowatość całkowita 0,75
średnica ziarna 5 mm
Obliczyć współczynniki retencji i współczynniki selektywności a (zdolność rozdzielczą) dla różnych składów fazy ruchomej.
Należy dokonać rozdzielenia tych izomerów z rozdzielczością 1,25. Jaka
powinna być wysokość półki teoretycznej H i zredukowana wysokość półki dla
2-HBA. Obliczenia przeprowadzić dla każdego składu fazy ruchomej. Posłużyć się
równaniem Purnella opisującym rozdzielczość pików.
Zadanie 6.2
Wartość mocy elucji rozpuszczalnika w chromatografii w układzie faz
odwróconych oblicza się na podstawie wzoru:
S’AB= fAS’A+ fBS’B
gdzie
S’ oznacza moc elucji
rozpuszczalnika
f - ułamek objętościowy rozpuszczalnika
|
Rozpuszczalnik |
S’ |
|
woda |
0 |
|
metanol |
3,0 |
|
acetonitryl |
3,1 |
|
aceton |
3,4 |
|
dioksan |
3,5 |
|
etanol |
3,6 |
|
izopropanol |
4,2 |
|
tetrahydrofuran |
4,4 |
W RP-HPLC rozdzielenie prowadzi się stosując jako eluent wodę z dodatkiem rozpuszczalnika
organicznego. W jakim stosunku objętościowym należy zmieszać:
a)
wode i metanol
b)
wodę i tetrahydrofuran.
aby otrzymany eluent miał taka samą moc jak mieszanina woda/acetonitryl (60/40).
Zadanie 6.3
Przy rozdzielaniu amidu kwasu salicylowego i kofeiny metodą RP-HPLC
otrzymano następujące współczynniki retencji
|
% metanolu |
30 |
35 |
40 |
45 |
50 |
55 |
|
ksal |
2,4 |
1,6 |
1,6 |
1 |
0,7 |
0,7 |
|
kkaf |
4,3 |
2,8 |
2,3 |
1,4 |
1,1 |
0,9 |
Wyjaśnij zmiany współczynników retencji
Jaka jest zaleta zastosowania eluentu o niskiej zawartości metanolu a jaka
wada?
Oblicz jak zmienia się moc elucji eluentu.
W jakich warunkach należy prowadzić rozdzielanie
Zadanie 6.4
Do wyznaczenia zależności pomiędzy
wysokością półki teoretycznej a prędkością przepływu zastosowano eluent o
składzie woda/ acetonitryl (50/50) oraz dwie kolumny C-18 12,5x0,46 cm i
kolumnę monolityczna C-18 10x 0,40 cm. W tabeli przedstawiono czasy retencji i
szerokości w połowie wysokości dla toluenu zarejestrowane dla obu kolumn.
Oblicz liczby półek teoretycznych N w zależności od zastosowanego przepływu
eluentu oraz wysokość półki teoretycznej. Wykreśl na jednym wykresie zależność
wysokości półki od przepływu dla obu kolumn. Przy jakiej optymalnej wartości
przepływu należy prowadzić analizę na każdej z kolumn.
|
Przepływ [ml/min] |
Kolumna monolityczna |
Kolumna C-18 |
||
|
Czas retencji [min] |
wh [min] |
Czas retencji [min] |
wh [min] |
|
|
0,25 |
28 |
0,691 |
48 |
1,318 |
|
0,5 |
14 |
0,33 |
24 |
0,639 |
|
1 |
7 |
0,156 |
12 |
0,314 |
|
2 |
3,5 |
0,074 |
6 |
0,165 |
|
3 |
2,33 |
0,05 |
4 |
0,119 |
|
4 |
1,75 |
0,039 |
3 |
0,100 |
|
5 |
1,4 |
0,033 |
2,4 |
0,088 |
|
6 |
1,17 |
0,029 |
- |
- |
|
8 |
0,88 |
0,024 |
- |
- |
Zadanie 6.5
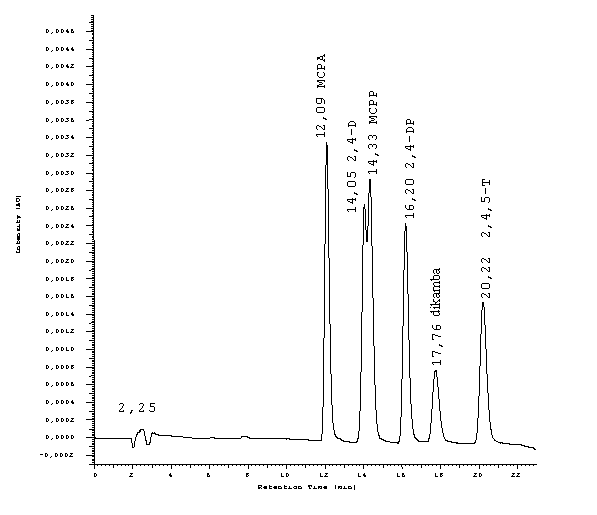
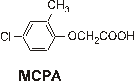
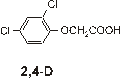
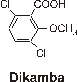
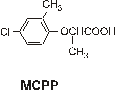
Rozdzielano 6 herbicydów: dikambę, MCPA, 2,4-D, MCPP, 2,4-DP, 2,4,5-T przy
zastosowaniu kolumny C-18 o długości 25 cm i średnicy 4,6 mm. Średnica ziaren
wynosiła 5 mm. jako eluent zastosowano mieszaninę kwasu octowego o stężeniu
43mM/L i acetonitryl.
Na podstawie chromatogramów dla każdego składu eluentu oblicz dla każdego
analitu współczynniki retencji k, współczynniki selektywności a, liczbę półek teoretycznych oraz rozdzielczość dla najsłabiej
rozdzielonych pików. Czas martwy tM=2,7 min. Proszę wykreślić na
jednym rysunku wykresy logk w funkcji % zawartości acetonitrylu.
|
|
|
|
kwas
4-chloro-2-metylofenoksyoctowy pKa=3,1 |
kwas 2,
4-dichlorofenoksyoctowy pKa=2,7 |
|
|
|
|
|
|
|
kwas
3,6-dichloro-2-metoksybenzoesowy pKa=1,9 |
kwas
2,4,5-trichlorofenoksyoctowy pKa=2,8 |
|
|
|
|
|
|
|
kwas 2-(4-chloro-2-metylo)fenoksypropanowy pKa=3,6 |
kwas 2-(2,4-dichloro)fenoksypropanowy pKa=2,7 |
35 % ACN
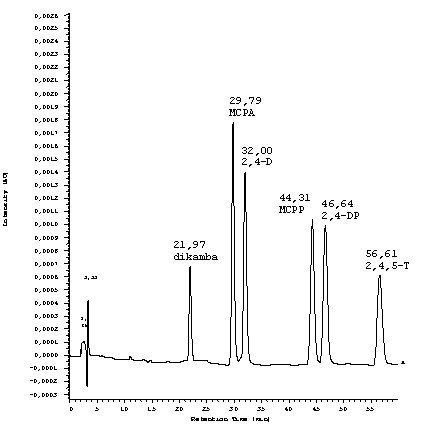
40 % ACN
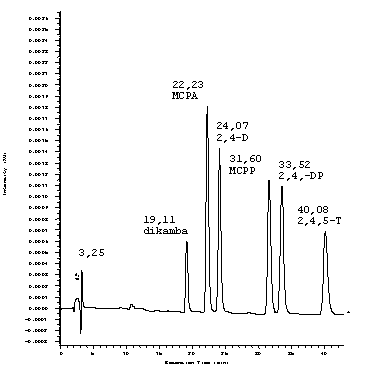
45 % ACN
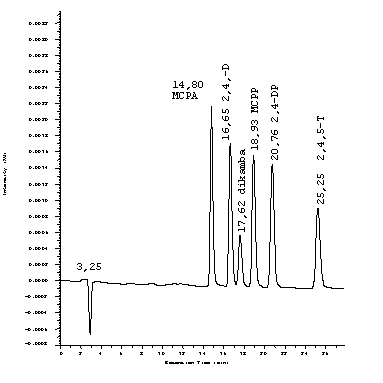
50 % ACN